2011河源中考化学考试说明大纲及样卷
(1)图中x的数值为 ,铝原子的核内质子数为 。
(2)铝具有很好的抗腐蚀性能,原因是(用化学方程式表示) 。
18.(6分)联合国气候变化框架公约《京都议定书》要求发达国家限制CO2排放,以控制日趋严重的温室效应。
(1)写出CO2的两种用途 、 。
(2)为了减慢大气中CO2含量的增加,以下建议可行的是 (填序号)。
①开发太阳能、水能、风能、地热能等新能源
②禁止使用煤、石油、天然气等矿物燃料
③大量植树造林,禁止乱砍滥伐
(3)为减少CO2的排放,科学家采取“组合转化”技术,将CO2和H2以一定比例混合,在一定条件下反应,生成乙烯(C2H4)和水。该反应的化学方程式为 。
19.(5分)某天然矿泉水标签中有如下文字叙述:“水质主要成分(mg/L):K+ 0.62-3.25 Na+ 18.7-29.8 Ca2+ 17.8-26.2 Cl― 14.2-30.8 硫酸根41.6-70.2 碳酸氢根184-261 pH 7.3”
(1)硫酸根离子的化学符号是 ;“Ca2+”中数字“2”的含义是 。
(2)该矿泉水显 (填“酸性”、“碱性”或“中性”)。
(3)日常生活中用 区别软水和硬水,可通过 方法降低水的硬度。
20.(4分)X、Y两种固体物质的溶解度曲线如下图所示。
回答下列问题:
(1)由X、Y两种物质的溶解度曲线可判断,溶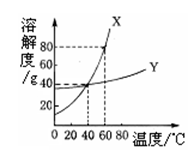
解度受温度影响较大的是 。
(2)40℃时,Y的溶解度为 g;60℃时,
把45g的X加入50g水中,充分溶解,得到
该温度下X的水溶液是 (填“饱
和”或“不饱和”)溶液。
(3)从Y的饱和溶液中提取Y,应采用的方法是 (填“冷却结晶”或“蒸发溶剂”)。
21.(10分)A~H是初中化学常见的物质。已知A为黑色固体单质,G为紫红色固体单质,B为红棕色粉末,F为黑色粉末,它们的转化关系如下图所示。请回答:
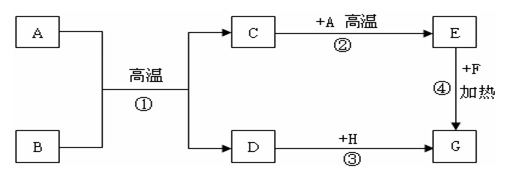
(1)B的化学式为 ,F的化学式为 。
(2)A、C、E三种物质中,具有还原性的是 、 (填化学式)。
(3)反应①的化学方程式为 ;写一个能实现反应③的化学方程式 。
(4)反应①~④中涉及的化学反应基本类型有 、 。
三、(本题包括2小题,共21分)
22.(12分)下图是实验室常用的实验装置,请回答有关问题:
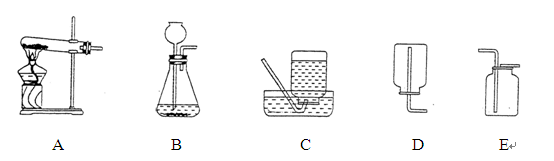
(1)装置C由导管、 和 (填仪器的名称)组成。
(2)实验室用H2O2和MnO2制取O2的化学方程式为 ,选用的发生装置是 (填序号,下同);若用KClO3和MnO2制取O2 时,则选用的发生装置是 。
(3)实验室制取CO2的化学方程式为 。若制得的CO2中混有HCl和H2O,提纯时用NaOH固体除去杂质,你认为这种方法 (填“可行”或“不可行”),理由是 。
(4)实验室制取H2应选用的收集装置是 或 。
23.(9分)某化学兴趣小组对“NaOH溶液与稀盐酸是否恰好完全反应”进行探究。请你参与他们的探究活动,并回答有关问题。
【实验探究】
(1)方案一:某同学按右图所示的方法先向试管中加入
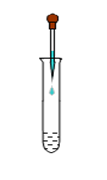
约2mL NaOH溶液,再滴入几滴酚酞溶液,溶液变
红。然后慢慢滴入稀盐酸,边滴边振荡,直至溶液
恰好变为 色,证明NaOH溶液与稀盐酸
恰好完全反应。
①请指出右图操作中的错误 。
②写出NaOH溶液与稀盐酸反应的化学方程式 。
(2)方案二:
|
实验步骤 |
实验现象 |
结论 |
|
取 取2mL NaOH溶液于试管中中,滴入一定量的稀盐酸,振振荡后加入镁条 |
若 |
稀盐酸过量 |
|
若没有明显现象 |
NaOH溶液与稀盐酸恰好完全反应 |
【实验反思】
(3)方案一在滴入稀盐酸的过程中,若观察到曾有少量气泡出现,请分析产生气泡的原因可能是 (写出一条即可)。
(4)有同学提出方案二不能证明NaOH溶液与稀盐酸恰好完全反应,其原因是 。为此,还需要选择 (填一种试剂),再进行实验即可。
【拓展应用】
(5)请举一例说明中和反应在生产生活中的应用 。
四、(本题包括2小题,共14分)
24.(6分)最近科学家研究确认,一些零食特别是油炸食品含有致癌物质丙烯酰胺(C3H5ON)。请回答:
(1)丙烯酰胺分子中碳、氢、氧、氮的原子个数比为 。
(2)丙烯酰胺的相对分子质量为 。
(3)丙烯酰胺中氮元素的质量分数为 (精确到0.1%)。
25.(8分)工业上用电解NaCl溶液的方法来制取NaOH、Cl2和H2,反应的化学方
程式为:2NaCl+2H2O ![]() 2NaOH+H2↑+Cl2↑。现取一定质量分数的
2NaOH+H2↑+Cl2↑。现取一定质量分数的
NaCl溶液214.6g进行电解,当NaCl完全反应时,生成0.4gH2。
(1)当NaCl完全反应时,生成Cl2的质量为 g,参加反应的NaCl的质量为 g。
(2)当NaCl完全反应时,所得NaOH溶液中溶质的质量分数为多少?(假设生成的Cl2和H2全部逸出)
2011河源中考化学考试说明大纲及样卷
2016年中考信息不断变化,www.91zhongkao.com 91中考网提供的中考成绩查询查分、录取分数线信息仅供参考,具体以相关招生考试部门的信息为准!



